文章來源公眾號:RNA派 作者:金豆
摘要
CAR-T療法在自身免疫性疾病中已經表現出持久緩解作用。
T細胞銜接器(T-cell Engager, TCE)療法在腫瘤治療中的藥效開始與 CAR-T 療法相匹敵。
TCE藥物在自身免疫性疾病中的療效有望與CAR-T療法相媲美。首先因為自免疾病需要清除的B細胞比腫瘤疾病要少,其次因為目前用于自免疾病的TCE藥物有很大改進空間。
關鍵問題解答
對于自身免疫疾病領域,一個核心問題是:能否為嚴重的自身免疫性疾病 (autoimmune disease, AID) 患者提供一種安全且可商業化的一次性療法來治愈他們的疾病?答案是肯定的,給出具體解釋之前,可以先看看以下問題。
1. 什么是自身免疫性疾病?
人體免疫細胞攻擊自身的細胞導致的疾病,往往由B細胞、T細胞和細胞因子驅動。通常由多種因素引起,但每種自免疾病都涉及特定的致病機制。
2. 什么是免疫重置?
通過消除致病性免疫記憶細胞來重置免疫系統,自身免疫性疾病患者即使在免疫系統再生后,也不再會有臨床癥狀。新生成的的B細胞和T細胞也不會具有致病性。
3. 自免疾病與淋巴瘤有何相似之處?
淋巴瘤是一種 B 細胞疾病(即 B 細胞過多)。該領域的藥物研發能夠幫助我們理解從 CAR-T 療法到 TCE等治療方式的進階路徑。此外,腫瘤學中的療效可能與 B 細胞的清除強度(自免疾病的關鍵因素)相關。我們還可以通過特定亞型(如濾泡性淋巴瘤、彌漫性大 B 細胞淋巴瘤(DLBCL)、B 細胞急性淋巴細胞白血病(B-ALL))來探究驅動療效的關鍵因素。
4. 自免疾病與淋巴瘤的差異之處?
相比之下,淋巴瘤的 B 細胞負荷更高,因此需要更高劑量的 CAR-T 療法、淋巴清除等聯合措施。腫瘤患者也更愿意承受更高的潛在毒性。
5. 何為淋巴細胞清除?
通過清除患者的免疫系統進行淋巴清除預處理,為 CAR-T 治療做前期準備。有人認為這有助于提高療效(畢竟清除的是B 細胞),但這種說法在自身免疫性疾病中可能并不成立(盡管高劑量的清淋在淋巴瘤中取得更好的療效)。
6. 是什么決定了TCE藥物的療效和毒性(如 CRS,細胞因子釋放綜合征)?
TCE藥物的療效 = 效價 × “血藥濃度vs作用時間”曲線下面積(AUC)。毒性 = 峰濃度(CMax)。
7. B 細胞清除如何影響免疫系統及其抗感染能力?
長期清除 B 細胞可能導致感染,但這不是治療的目的。最終目的是在免疫重置后實現免疫系統的重建。
8. 區分自免疾病的亞型種類是否重要?
當然。如果疾病由 T 細胞介導,那么清除所有 B 細胞并不會起效。紅斑狼瘡是一個典型例子,它由 B 細胞異常引起且治療難度大。而其他疾病如重癥肌無力由抗體引起,則不需要進行 “免疫重置”。
要想免疫重置?
Car-T療法切實有效
CAR-T 療法的成功:George Schett發表的具有里程碑意義的論文顯示,采用 CAR-T 療法治療難治性自身免疫病的患者,5 年緩解率高達 92%。患者經一次性治療后實現了治愈。那么這其中,又是怎么會想到采用毒性大、新一代的CAR-T腫瘤治療方式創建“免疫重置”來治療自身免疫性疾病的呢?免疫重置的概念始于20世紀80年代的造血干細胞移植(Hematopoietic Stem Cell Therapy,HSCT)。在那個年代,人們用造血干細胞移植來治療嚴重的自身免疫性疾病。
造血干細胞移植通過免疫重置發揮作用
造血干細胞療法通過淋巴消融(Lymphoablation)清除人體自身的免疫系統(在自身免疫病中處于過度活躍狀態),并通過回輸初始干細胞實現免疫系統的 “重置”。該療法于 1995 年守次被提出,1996 年出現守例臨床病例報告。醫生們觀察到它能誘導疾病 緩解,于是聯合開展研究以追蹤療效。在 15 年時間中,約 1000 名自免患者接受了造血干細胞移植,主要用于治療多發性硬化癥、系統性硬化癥和紅斑狼瘡。早期試驗顯示,約 40% 的患者實現在 5 年內無病生存,總生存率達 80%,但不同醫療中心的治療效果差異較大。
造血干細胞移植 (HSCT) 通過以下步驟來誘導“免疫重置”:1.殺死體內所有的免疫細胞;2.給患者回輸新的干細胞;3.靜靜祈禱這種方法起效。
但這種方法存在重大問題。造血干細胞移植(HSCT)更像是一項僅由專業學術醫療中心的醫生們掌握的特殊技藝,并非可直接商業化的治療方法。然而,它仍然為我們提供了概念驗證。盡管有些患者死于移植并發癥,盡管只有40%的患者獲得了5年緩解,盡管它的療效高度依賴于醫療中心的水平,但造血干細胞移植證明了免疫重置是可行的,可以通過回輸干細胞,為重癥患者誘導疾病緩解。甚至對于重癥系統性硬化癥,該療法已被納入保險覆蓋范圍。
CAR-T療法登場
用于治療自身免疫性疾病的CAR-T療法與造血干細胞移植(HSCT)類似,但靶向性更強。CAR-T療法并非采用徹低的淋巴消融,而是使用淋巴細胞清除術(Lymphodeletion)來減輕免疫細胞負擔,然后輸注CAR-T療法靶向殺傷所有表達特定靶點(最初是CD19靶點)的細胞。
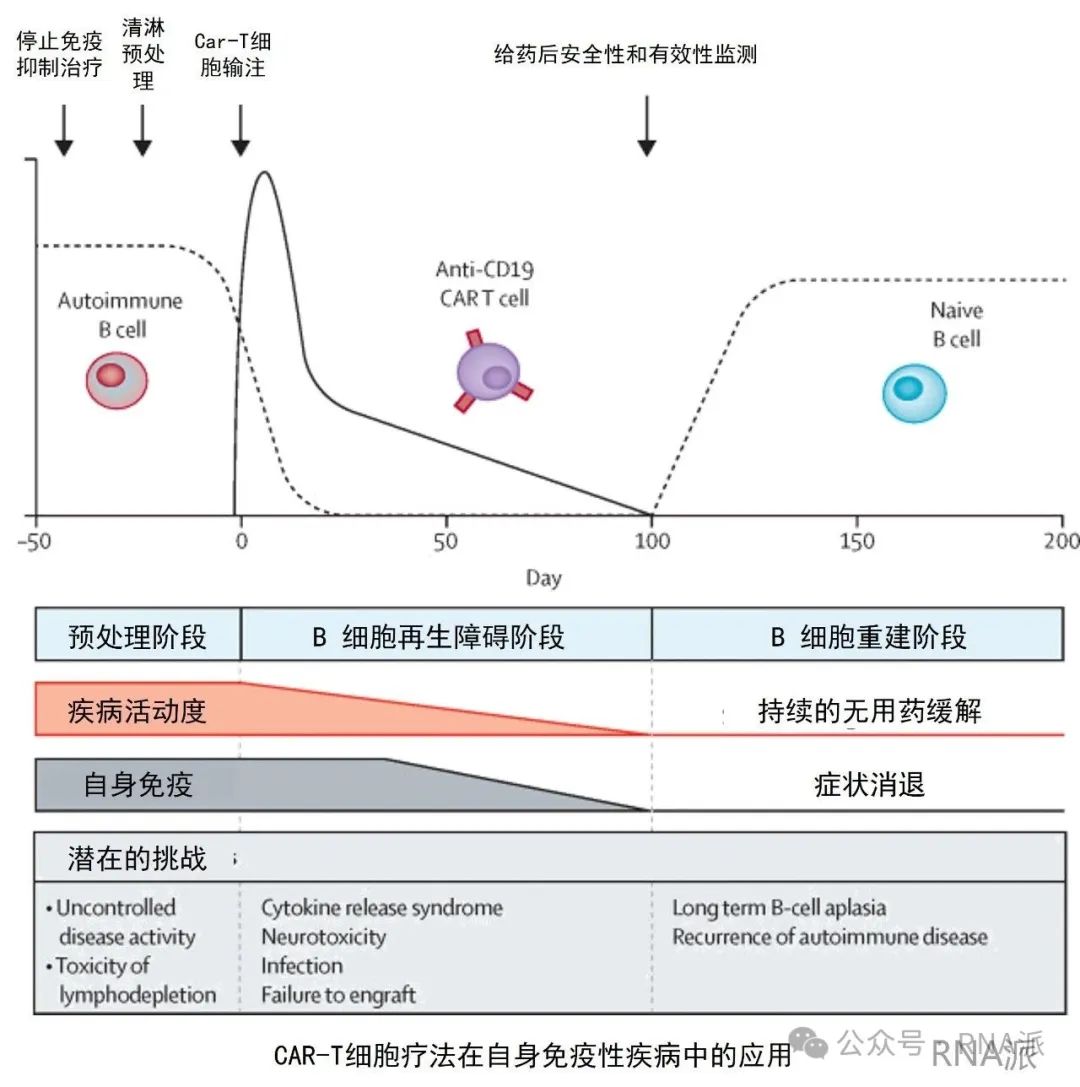
從造血干細胞移植(HSCT)到嵌合抗原受體 T 細胞(CAR-T)療法的發展,背后反映的是淋巴瘤治療的進階之路。其標準的一線治療是 R-CHOP 方案(利妥昔單抗、環磷酰胺、多柔比星、長春新堿和潑尼松),治療失敗后采用干細胞移植。CAR-T 療法通常用于三線及更后線的治療,且應用階段正逐漸提前。CAR-T治療方法的演進與腫瘤學療法進階之路的類似之處將會晚點討論。
對于自身免疫性疾病,CAR-T 療法并非像造血干細胞移植那樣摧毀整個免疫系統,而是靶向特定的致病性克隆。從理論上講,我們只需 “重置” CD19 陽性細胞。需要注意的是,CD19 陽性細胞處于發育的最早階段。然而,成熟的 B 細胞或 T 細胞并不表達 CD19,因此 CD19 CAR-T 不會影響這些細胞。在癌癥治療中,這不是問題,因為此類疾病由 B 細胞介導。
但對于自身免疫性疾病(AID),靶向 CD19 似乎并不合理:自身免疫性疾病通常是多因素導致的,涉及 T 細胞。有些自身免疫性疾病由 B 細胞介導,但對于大多數難以治療的情況,T 細胞和 B 細胞之間的相互作用尚不清楚。僅用 CAR-T 療法是否仍能有效清除體內足夠多的 B 細胞,以誘導免疫重置呢?由此,這里需要提出兩個不同的問題。一是,如果我們僅通過靶向 CD19 + 細胞就能重置 B 細胞譜系,這是否足以在某些自身免疫病(AIDs)中誘導持續應答?二是,CAR-T 療法能否達到淋巴消融的效果?(患者是否真的需要達到這種效果?)
這兩個問題的答案都是肯定的。George Schett近期發表的數據證實了這一理論的可行性:CAR-T療法能夠在狼瘡患者中誘導免疫重置,進而實現臨床緩解。在腫瘤學領域,CAR-T 療法對 B 細胞的清除效果堪比淋巴消融和移植。但這種具有概念驗證意義的開創性療法仍存在不足。
以下是自體 CAR-T 療法存在的不足之處: 不足點 1:適合接受治療的難治性疾病患者群體規模過小。 用于自身免疫病的自體 CAR-T 療法在商業化上是存在瓶頸的。學術醫療中心可以借助 CAR-T 療法進行概念驗證,但生產制造方面的限制、需要進行清淋預處理以及患者自身素質等,使得傳統 CAR-T 療法難以實際應用。一項關于治療資格的研究納入了 1800 名系統性紅斑狼瘡(SLE)患者,結果顯示僅 54 人符合CAR-T治療條件,最終僅有 2 人接受了治療 —— 沒錯,只有 2 人。從疾病嚴重程度來看,符合治療條件的患者僅占千分之一。 根據系統性紅斑狼瘡在美國患病人群32 萬人及歐洲患病人群15萬人來算,二者合計按理來說約有 500 名符合條件的患者。這些患者需要滿足病情嚴重、處于活動期、癥狀表現符合特定要求等條件,即便完荃符合所有標準,他們也無法在醫院停留那么久。因為接受輸注前需要住院一周,期間會徹低抑制患者整個免疫系統,之后進行 CAR-T 治療。接受治療后還需要有人長期照顧,因為患者會極度虛弱,幾乎無法行走,還得頻繁去看醫生。由此可能導致患者的家人需要放下工作來陪護照顧。 自身免疫性疾病畢竟不同于那些5 年生存率極低的侵襲性 B 細胞淋巴癌,自免疾病患者還能過著還算正常的生活,當然有些人內心也清楚,可能有一天,長期服用的一些藥物、腎臟損傷和慢性疼痛會奪走他們的生命。 不足點 2:成本與生產制造 目前還無法生產足夠劑量的CAR-T供應。例如該領域的頭部企業——Cabaletta 生物公司到 2027 年的計劃年產量才能達到 1000 劑。 自體 CAR-T 療法的實施需要先在醫院進行為期一周的治療,包括淋巴清除步驟,這種流程導致治療數量難以放量。 難治性自身免疫病患者不像癌癥患者那樣有直接的渠道對接大型醫療中心,很多只能終身與癥狀為伴。 |
那么問題來了。
問題 1:自免領域未被滿足的臨床需求是否真的存在?
答案是存在,且十分顯著。自身免疫病雖不會 “快速” 致命,卻以慢性、漸進的方式嚴重侵蝕患者的生命質量與長期健康:1)疾病通過反復的 “發作(flares)” 引發持續炎癥,伴隨疼痛、疲勞、器官損傷(如狼瘡導致的腎炎)等癥狀,逐步消耗患者的 “生命力”;2)長期使用免疫抑制劑控制病情,又會帶來感染風險增加、骨質疏松、代謝紊亂等副作用,進一步降低生活質量;3)即使患者短期內不會面臨死亡,病程進展往往不可逆轉 —— 例如狼瘡患者最終可能因腎衰竭需要終身透析,類風濕關節炎患者可能因關節畸形喪失行動能力。
現有治療方案(如激素、免疫抑制劑)多以 “控制癥狀” 為目標,無法跟治疾病,且對部分難治性患者效果有限。這些患者在漫長病程中承受的痛苦、功能喪失和器官損傷風險,正是亟待解決的 “未被滿足的需求”。
問題2:患者能否避免清淋(Lymphodepletion)預處理?
這應該是存在可能性的,但需權衡療效與安全性,且依賴技術突破。目前大家認為清淋的核心作用包括:1)為 CAR-T 細胞 “騰空間”:清除體內現存的免疫細胞(尤其是 T 細胞),減少對 CAR-T 細胞的競爭,使其更易定植、增殖;2)優化微環境:通過清除細胞釋放的細胞因子(如 IL-15),為 CAR-T 細胞創造更有利的存活與活化條件;3)高強度的清除往往會產生更理想的細胞因子譜,這與更長的無進展生存期(PFS)和更好的治療效果相關。但清淋并非什么一般的藥片:它需要長達一個月的住院治療,會把患者變成一個沒有免疫系統的 “玻璃人”。如果在細胞療法中可以避免,就應該盡量省去。
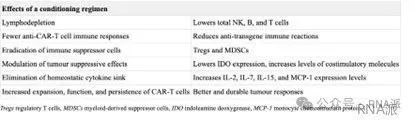
一個有趣的難題擺在眼前:如果CAR-T療法的目標是殺死患者的免疫細胞,而清淋療法預處理恰恰是在在耗竭免疫系統,那么清淋的作用是否遠不止“調節患者給藥條件”?有人認為,清淋處理也有助于提高療效。
這一理論得到了腫瘤學數據的支持。CHOP 化療是常用的一線淋巴瘤清淋療法,并非完荃免疫系統消融療法,但仍能誘導緩解。高劑量的清淋通常能帶來更好的療效。但自身免疫性疾病的數據則有所不同。
高劑量的清淋預處理不一定對CAR-T療法治療自免疾病的療效有幫助,原因有幾個。
1.單用清淋療法無法在自免疾病患者中誘導臨床反應。有研究嘗試過用淋巴細胞清除療法來誘導自免患者的免疫重置,但根本不起作用。最近,George Schett用淋巴細胞清除療法治療了一位復發的CAR-T患者,但未見臨床反應:“盡管進行了滿劑量的淋巴細胞清除治療,但在自身免疫性疾病中仍未觀察到臨床反應。”
2.降低疾病負擔:清淋在腫瘤學中發揮作用的部分原因是它能提高 CAR-T 細胞的數量和持久性。通常希望 CAR-T 細胞在癌癥治療中能達到較高的初始峰值和長期持久性。但 Schett 的數據卻表明,在自身免疫性疾病中情況恰恰相反:CAR-T 細胞在初始峰值之后,數量會逐漸降至 0,但仍然能看到持續的療效。因此自免疾病可能不需要 CAR-T 細胞永遠存在。
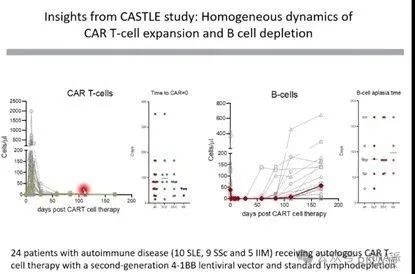
3. 我們已經從FATE Therapeutics 公司對未清淋的系統性紅斑狼瘡患者進行CAR-T治療結果中看到了概念驗證。雖然他們只展示了1例患者的結果(尚需要更多患者數據),但這在一定程度上證明了無需清淋方案在臨床PoC中的有效性。遺憾的是,給藥后的B細胞清除并不撤底,這意味著需要更高劑量或療效更強的藥物才能誘導持久的臨床反應。
問題3:為什么應該針對 CD19靶點,而不是 CD20靶點?
CD20 是免疫耗竭的原始靶點。利妥昔單抗是一種靶向 CD20 的抗體,通過減少致病性B 細胞來治療系統性紅斑狼瘡,但仍有一些患者用藥后會復發,因為 CD20 只在少部分的細胞亞群中表達。對利妥昔單抗治療有響應然后又復發的患者通常仍有 CD20 陰性、CD19 陽性的 B 細胞在體內游走。除此之外,CD19 CAR-T 可以在利妥昔單抗之后起作用。另外,盡管CD20xCD3 T細胞結合雙特異性的莫妥珠單抗在淋巴瘤中效果更好,但最近治療狼瘡患者的莫妥珠單抗(CD20 TCE療法)的數據比所有 CD19 T 細胞接合劑的數據都要差。人們已經看到 CD20數據一再令人失望,這不是藥物問題,而是靶點問題。所有概念驗證數據都支持將 CD19 作為靶點。所以如果我們要重置免疫系統:有什么理由不選擇發育譜系中最早的細胞呢?
問題4:B細胞清除率與臨床療效的關系。
臨床試驗中使用B細胞清除率作為療效的替代終點,是因為臨床上的癥狀(例如患者的自我感受)可能會受到安慰劑的影響。臨床表征是最終的目標,誘導持久的臨床癥狀緩解并非是虛的,但這類早期臨床數據難以解讀。因此,B細胞清除率與臨床癥狀緩解的相關性是一個很好的替代指標。
TCE療法及來自腫瘤學的啟示
在腫瘤學中,所有CAR-T療法(包括自體或同種異體、T 細胞或 NK 細胞、伴隨清淋處理或不作清淋處理)之后的下一代療法是 T 細胞接合器。無論如何,治療目標是 清除致病性的B 細胞,方法并不重要。
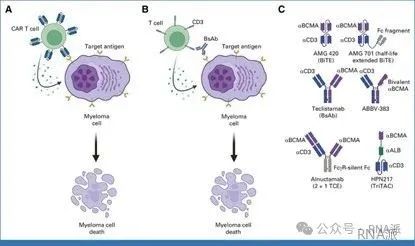
二者的不同工作原理
CAR-T療法通過輸注外部經過編輯的T細胞來殺傷癌細胞,而TCE療法(或稱bispecific T cell engager,BiTE)則利用患者自身的T細胞來殺傷癌細胞。TCE的一端是靶標,另一端是CD3部分。靶標會與靶細胞結合,并募集T細胞來殺傷癌細胞。CAR-T = 表面具備特異性靶向功能的T細胞。TCE = 特異性地募集自身T細胞
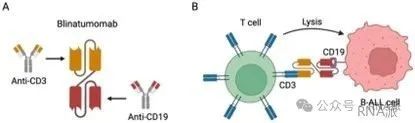
Blinatumomab 藥物作用機制
TCE療法通常在醫院通過靜脈注射給藥,以觀察患者是否出現“細胞因子風暴”(CRS,免疫系統激活會導致發燒、發冷等癥狀)或免疫效應細胞相關神經毒性綜合征(ICANS)。TCE療法的給藥周期固定,直至病情緩解或疾病進展。TCE療法并非一次性給藥療法。它的治療療程時長可以適時調整。
在濾泡性淋巴瘤中莫妥珠單抗 8 個療程的治療可獲得 70% 的 CR。目前已經有四種 TCE 藥物獲批用于治療多種淋巴瘤。但能治療一種淋巴瘤不等于能治療所有淋巴瘤。有些淋巴瘤的疾病負擔更重,其在血液中的增殖或分布比淋巴組織中的更高。高增殖率的組織淋巴瘤比惰性的血液淋巴瘤更難治療,因此對于像彌漫大B細胞淋巴瘤這樣的疾病,CAR-T療法是守選(通常更有效,但風險更高)。T 細胞在血液中隨時可用于殺傷腫瘤細胞,而組織源性疾病則更難跟除。
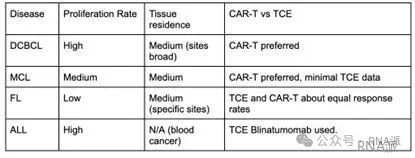
但這種療效對比數據并非治療方式本身的局限性,而是藥物設計的問題。合適的 TCE療法能夠達到甚至超越 CAR-T 療法的療效。治療的目標是清除B細胞。只有在組織中更有效地清除B細胞,才能帶來更高的療效。
Blinatumomab 的啟示—— 我們可以設計更好的 TCE
博納吐單抗(Blinatumomab)已獲批用于治療急性淋巴細胞白血病(ALL),但在非霍奇金淋巴瘤(NHL)中的研究卻未獲成功。
有研究分析了blinatumomab在非霍奇金淋巴瘤中的PK和PD。

劑量與穩態濃度呈線性關系

B 細胞清除率與穩態濃度呈對數關系。
數據指出非霍奇金淋巴瘤治療所需的蕞低劑量為 47 微克 / 平方米 / 天,這幾乎是美國FDA批準的癌癥治療劑量的兩倍。博納吐單抗(Blinatumomab)也許可以用于治療非霍奇金淋巴瘤(NHL),但其療效受到耐受性的限制。研究也曾嘗試將劑量提高至 112 微克,但臨床試驗中途退出的患者太多。
非霍奇金淋巴瘤 (NHL) 同樣屬于組織源性疾病,需要深度清除組織中的腫瘤細胞,然而博納吐單抗(Blinatumomab)無法有效穿透組織。外周血 B 細胞的清除相對容易,但從動力學角度來看,其最大療效始終未能達到。通過劑量反應曲線可知,即使藥物濃度達到 10000 皮克 / 毫升,療效仍有待提升。
Blinatumomab并非一款玩美的藥物:盡管它作為開創性療法,比大多數其他 TCE療法早數年獲批,但存在諸多問題:
1.給藥頻率每天一次,半衰期為 5 小時。
2.該藥物的組織穿透性較差(因此僅獲批用于急性淋巴細胞白血病)。
3.它缺乏 Fc 效應子功能。作為一種 CD3-CD19 雙特異性抗體,它無法激活與抗體相關的功能,這限制了療效。
因此,更優質的 CD19 雙特異性抗體是有可能研發出來的。阿斯利康的 TNB-046 在 5 例未接受過 CAR-T 治療的患者中顯示出 80% 的緩解率,在接受過 CAR-T 治療的患者中緩解率為 36%。這就像在戰場上,一把守槍在大面積火炮(CAR-T 療法)打擊后仍能造成對殘存敵人的殺傷效果。

從這些數據中,我們得出一個重要結論:Blinatumomab并非最佳的 TCE療法。無論是在腫瘤領域還是自身免疫性疾病領域,我們都能研發出更優質的藥物。
腫瘤疾病不是自身免疫性疾病
我們不能將腫瘤學中的療效經驗直接應用于自身免疫性疾病。“腫瘤疾病中使用TCE的持久性很差,這些數據遠不及CAR-T數據”, 在用 TCE療法清除 B 細胞后,B 細胞會再生。但自身免疫性疾病有所不同。
B 細胞淋巴瘤由 “天生” 具有增殖特性的 B 細胞驅動,而癌癥本質上是一種增殖性疾病。自身免疫性疾病則不同:
自身免疫性疾病中的 B 細胞負荷低得多,因此我們需要清除的 B 細胞數量更少;到目前為止,在腫瘤學中,給藥劑量尚未達到治療水平;由于安全性顧慮,半衰期短的藥物其潛在療效受到限制;組織穿透性不足(即博納吐單抗存在明顯缺陷)。因此自身免疫疾病不需要像 CAR-T 這樣的 “火炮”,用相對溫和的療法治療是可行的。
TCE療法的安全性和有效性
TCE的安全性如何?存在細胞因子風暴(CRS)風險嗎?
TCE比 CAR-T 安全得多,但我們仍需關注兩點:1)藥物本身相關的 CRS / 免疫效應細胞相關神經毒性綜合征(ICANS);2)B 細胞清除后引發的感染。細胞因子釋放綜合征(CRS)是一種免疫介導的副作用,由 T 細胞激活引發,會導致細胞因子立即過量釋放,進而引起發熱、寒戰等免疫相關癥狀。CRS 在守次給藥后最為常見,其發生與藥物對 CD3 和 CD19 的相對親和力有關。CD3 在 T 細胞上表達,因此對 CD3 的親和力越高,T 細胞激活就越強,CRS 的發生率也就越高。
“給抗體設計一個高親和力的腫瘤靶向臂(CD19)并搭配低親和力的 CD3 臂,可形成一種動力學層級 —— 即‘先標記靶點,再招募T 細胞’—— 這樣既能維持腫瘤殺傷能力,又能降低細胞因子峰值。”
CRS 的第二個影響因素是體內初始藥物濃度:守次輸注后發生的 CRS 由峰濃度(Cmax,即最大濃度)驅動。這就是現實臨床中醫生會逐步增加劑量的原因 ——試驗從小劑量開始,以規避安全風險,因為守次給藥可能引發細胞因子激增。
為降低 CRS 風險,我們需要藥物具備以下特性:較高的 CD19 與 CD3 相對親和力比值,以及較低的初始濃度峰值。
免疫效應細胞相關神經毒性綜合征(ICANS)的毒性機制尚不完荃明確。說實話,目前可以推測 ICANS 的風險,但患者臨床試驗數據才是判斷潛在安全性問題的更可靠依據。此外有人認為這類療法會抑制免疫系統并引發感染。但也許這并非值得擔憂的問題。首先適合這類療法的患者本就需要終身服用長期類固醇或其他免疫抑制劑。而且CD19 不在成熟漿細胞上表達,因此患者能維持疫苗的抗體滴度。此外重置免疫系統會促使 B 細胞再生。
TCE在自身免疫性疾病中的數據
TCE療法被用于治療嚴重 RA患者、系統性硬化癥和狼瘡患者、抗合成酶綜合征。(大多數使用 blinatuomab,其它使用 A-319)。

在每項試驗中,與腫瘤學數據相比,自免疾病采用的劑量較低,但仍能誘導疾病緩解。人們會因為這些數據對TCE療法提出質疑,因為患者出現復發、B 細胞清除效果反彈等情況。但這樣的看法也許是錯誤的,因為這里使用的是在癌癥治療中效果不佳的藥物,不僅降低了劑量,還將其用于高度難治性自身免疫病患者。這些并非是理想情況下的數據,但我們仍觀察到了藥物起效的跡象:臨床應答和 B 細胞清除均有出現。肌肉活檢顯示組織內B細胞清除效裹先著(盡管尚無淋巴組織的數據)。
總結
CD19 CAR-T 療法可誘導免疫重置,在 CAR-T 細胞消失且 B 細胞再生后,患者仍能維持臨床緩解。
從腫瘤學療法的啟示來看,順理成章的下一步是研發 CD19 TCE療法,但博納吐單抗采用靜脈給藥,組織穿透性差,且受毒性限制。
其他在研的 CD19 TCE療法在癌癥治療中比現有方法更有效,這證明我們能夠設計出更優質的藥物。
即便劑量不足,博納吐單抗在自身免疫病中仍顯示出療效,這支持了 “自身免疫病中 B 細胞負荷較低” 的理論。
效價更高、采用皮下給藥且在淋巴瘤中已有初步療效證據的藥物,有望在自身免疫病中實現免疫重置(盡管研發周期較長)。
點擊藍字 關注我們
自免疾病的下一站,TCE還是CAR-T?
相關產品
免責聲明
- 凡本網注明“來源:化工儀器網”的所有作品,均為浙江興旺寶明通網絡有限公司-化工儀器網合法擁有版權或有權使用的作品,未經本網授權不得轉載、摘編或利用其它方式使用上述作品。已經本網授權使用作品的,應在授權范圍內使用,并注明“來源:化工儀器網”。違反上述聲明者,本網將追究其相關法律責任。
- 本網轉載并注明自其他來源(非化工儀器網)的作品,目的在于傳遞更多信息,并不代表本網贊同其觀點和對其真實性負責,不承擔此類作品侵權行為的直接責任及連帶責任。其他媒體、網站或個人從本網轉載時,必須保留本網注明的作品第一來源,并自負版權等法律責任。
- 如涉及作品內容、版權等問題,請在作品發表之日起一周內與本網聯系,否則視為放棄相關權利。
 手機版
手機版 化工儀器網手機版
化工儀器網手機版
 化工儀器網小程序
化工儀器網小程序
 官方微信
官方微信 公眾號:chem17
公眾號:chem17
 掃碼關注視頻號
掃碼關注視頻號



















 采購中心
采購中心